胸腺素β4的應(yīng)用與市場前景
2020-06-28 08:25:21
linda
1089
胸腺素β4(Thymosinβ4�����,Tβ4)是1966年Goldstein等首先從小牛胸腺中提取出的促淋巴細(xì)胞生成因子�����,是人體內(nèi)廣泛存在的一種43個氨基酸組成的肽類物質(zhì)����。天然Tβ4由43個氨基酸組成,其氨基酸序列和二級結(jié)構(gòu)如下圖所示�����。Tβ4的結(jié)構(gòu)中缺乏疏水性氨基酸,屬于水溶性蛋白��。
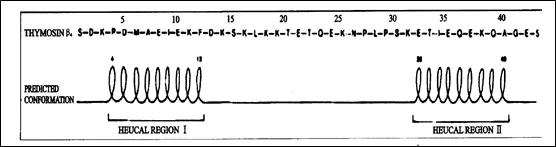
Tβ4氨基酸序列和二級結(jié)構(gòu)圖���,來源于文獻(xiàn)《胸腺素β4的研究與開發(fā)進(jìn)展》,中國生物醫(yī)藥技術(shù)�����,2009年2月第4卷第1期
Tβ4是人體內(nèi)主要的肌動蛋白調(diào)節(jié)因子之一����,具有廣泛的生物學(xué)活性,與細(xì)胞骨架平衡��、炎癥反應(yīng)���、創(chuàng)傷愈合��、血管再生���、細(xì)胞調(diào)亡�、角膜及心肌修復(fù)等密切相關(guān)����。眾多研究結(jié)果顯示,Tβ4與很多生理過程緊密相關(guān)��,具有非常廣泛的應(yīng)用前景��,可用于心肌梗死(Myocardialinfarction簡稱MI)�、干眼癥、角膜損傷����、壓迫性潰瘍、口腔粘膜炎癥以及肺損傷等多種疾病的治療�����。目前針對Tβ4的開發(fā)已經(jīng)進(jìn)入臨床研究階段��,擬用于治療心肌缺血-再灌注損傷(MyocardialIschemia Reperfusion Injury��,MIRI)����、急性肺損傷(acutelung injury, ALI)�����、干眼癥�����、角膜損傷����、壓迫性潰瘍等���,其中美國RegeneRX公司研發(fā)的重組胸腺素β4已經(jīng)處于臨床III期階段。心肌梗死��,舊稱心肌梗塞����,是一種急性及嚴(yán)重的心臟狀態(tài)。急性心肌梗死(acutemyocardial infarction�����,AMI)是在冠狀動脈病變的基礎(chǔ)上���,發(fā)生冠狀動脈血供急劇減少或中斷�����,使相應(yīng)的心肌嚴(yán)重而持久地急性缺血所致的部分心肌急性壞死�����。AMI是一組由急性心肌缺血引起的臨床綜合征�����,主要包括ST段抬高型心肌梗死(STEMI)和非ST段抬高型心肌梗死(NSTEMI)�。AMI的治療方法主要有經(jīng)皮冠狀動脈介入(PCI)、溶栓�、和冠脈旁路搭橋術(shù)等。臨床上��,PCI發(fā)揮著挽救AMI患者生命的重要作用��,提高了患者的生存率�,但同時也是MIRI的重要誘因。MIRI的形成涉及一系列復(fù)雜的病理過程���,包括氧自由基生成過多��、細(xì)胞內(nèi)鈣離子超載�、生理pH值快速恢復(fù)、mPTP開放����、炎癥反應(yīng)等[1],最后出現(xiàn)不可逆的細(xì)胞凋亡和壞死�����。目前����,尚無有效治療MIRI的藥物獲批上市�����,臨床上關(guān)于MIRI的評估與治療是近年來的研究熱點之一���,如何充分和有效地利用已知的MIRI機(jī)制來預(yù)防或治療缺血性心腦疾病�����,是國內(nèi)亟待解決的未滿足臨床需求�����。目前關(guān)于減輕MIRI的研究中涉及到的防治策略包括缺血預(yù)適應(yīng)�、增加局部腺苷濃度、防止細(xì)胞內(nèi)鈣超載��、抑制mPTP開放��、減少ROS生成��、NO代謝���、心臟停搏液的代謝添加劑���、抗炎癥反應(yīng)、吸入性麻醉劑���、舒張血管��、缺血后適應(yīng)等[2]�。據(jù)國家心血管疾病醫(yī)療質(zhì)量控制中心公布的數(shù)據(jù)統(tǒng)計�,2009-2018年冠心病患者接受PCI手術(shù)例數(shù)的年復(fù)合增長率為16.68%,2014-2018年的年復(fù)合增長率為16.26%。由于人口老齡化��、我國冠心病患者數(shù)量增加��。近年來��,我國國民健康意識不斷提高�����,人均可支配收入不斷提升�����,醫(yī)療資源也日益豐富��,醫(yī)保報銷比例逐步上升����。此外�,隨著國內(nèi)區(qū)縣級醫(yī)院PCI能力逐步提高,臨床醫(yī)生技術(shù)水平不斷提高��,我國主動脈疾病的檢出率將不斷提高����,包括STEMI患者在內(nèi)的急診PCI比例將進(jìn)一步提升���,預(yù)期有關(guān)數(shù)量將會保持穩(wěn)定增長,參考?xì)v史增長情況����,假設(shè)2019-2025年我國冠心病患者接受PCI手術(shù)例數(shù)的年復(fù)合增長率為15%,預(yù)計2025年我國有243萬例冠心病患者的PCI手術(shù)[3]��。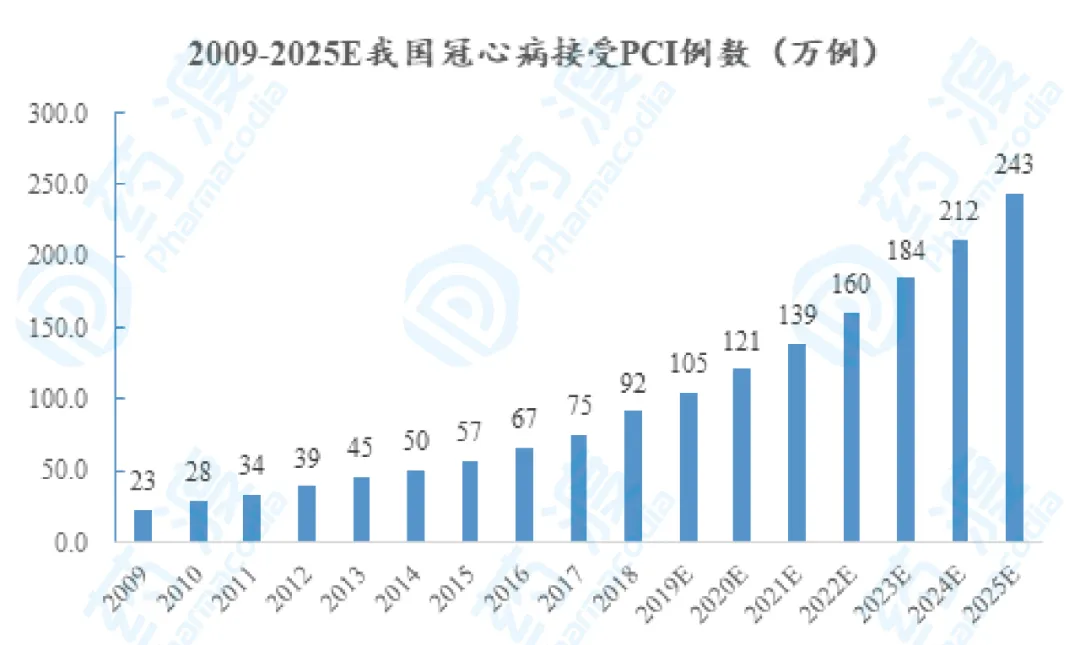
2009年-2025年我國冠心病接受PCI例數(shù)數(shù)據(jù)來源:《中國心血管病報告2018》���,國家心血管疾病醫(yī)療質(zhì)量控制中心�,藥渡分析根據(jù)2019年4月27日��,在第二十二屆全國介入心臟病學(xué)論壇(CCIF2019)上����,北京大學(xué)第一醫(yī)院、中國心血管健康聯(lián)盟副主席霍勇教授代表國家心血管疾病醫(yī)療質(zhì)量控制中心發(fā)布冠心病介入治療數(shù)據(jù)�,2018年接受PCI手術(shù)的冠心病患者中STEMI患者共23.8萬例,占比為26%�����,NSTEMI患者共9.2萬例,占比為10%�,即2018年接受PCI手術(shù)的冠心病患者中AMI患者占比共計36%。據(jù)《中國心血管病報告2018》�����,2017年接受PCI手術(shù)的冠心病患者中AMI患者占比共計35%����。同時國家心血管疾病醫(yī)療質(zhì)量控制中心還發(fā)布了我國STEMI患者直接PCI的比例由2009年的29.76%增長到2018年的45.94%,其中近五年的增長速度較快��,說明PCI手術(shù)在AMI患者�,尤其是STEMI患者治療中的地位愈加重要。假設(shè)按照2018年AMI接受PCI手術(shù)占比為36%估計��,則2019年我國有27.4萬例AMI患者接受PCI手術(shù)�,隨著冠心病患者接受PCI手術(shù)的增多,2025年將有87.6萬例AMI患者接受PCI���,詳見下圖���。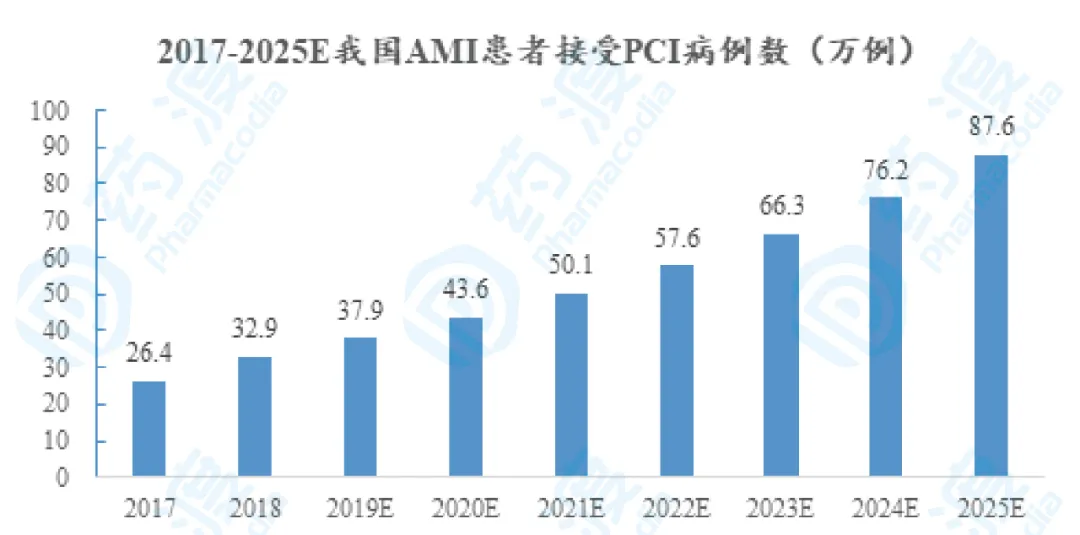
2017-2025E我國AMI患者接受PCI病例數(shù)數(shù)據(jù)來源:《中國心血管病報告2018》��,國家心血管疾病醫(yī)療質(zhì)量控制中心,藥渡分析目前針對MIRI的研究還在不斷的完善����,國內(nèi)外沒有關(guān)于MIRI發(fā)生率的準(zhǔn)確統(tǒng)計。MIRI可引起患者心律失常��、梗死面積擴(kuò)大和持久性心室功能低下等狀況����。隨著對MIRI發(fā)病機(jī)制的認(rèn)識,未來MIRI治療藥物可能會與PCI術(shù)后抗栓治療上升至同等地位���。據(jù)文獻(xiàn)[4]���,PCI術(shù)后的AMI患者如并發(fā)心力衰竭,則其住院費用增加7232.41元�����,而PCI術(shù)后AMI患者發(fā)生MIRI會發(fā)生惡性心律失常�����、心肌頓抑����、梗死面積擴(kuò)大��、持久性心室收縮功能低下甚至死亡等����,發(fā)生MIRI的AMI患者其預(yù)后更加難以處理���,治療費用應(yīng)更高����。保守估計下����,參考并發(fā)心力衰竭時增加的治療費用作為發(fā)生MIRI的AMI患者的治療費用,綜上��,MIRI治療的理論市場規(guī)模在2025年將達(dá)到63.4億元����。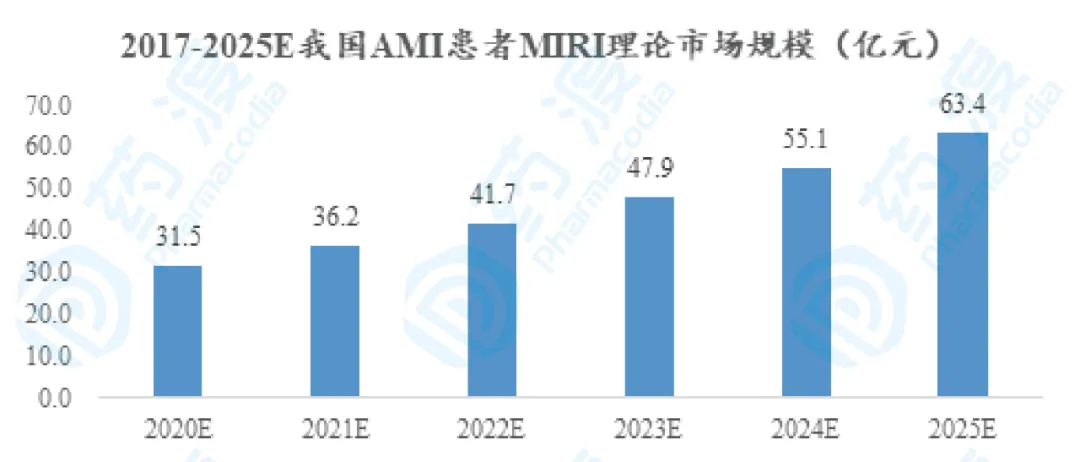
2020E-2025E我國AMI患者M(jìn)IRI理論市場規(guī)模(億元)急性肺損傷(acutelung injury, ALI)是指各種直接和間接致傷因素導(dǎo)致的肺泡上皮細(xì)胞及毛細(xì)血管內(nèi)皮細(xì)胞損傷,造成彌漫性肺間質(zhì)及肺泡水腫�,導(dǎo)致的急性低氧性呼吸功能不全。以肺容積減少��、肺順應(yīng)性降低、通氣/血流比例失調(diào)為病理生理特征�����,臨床上表現(xiàn)為進(jìn)行性低氧血癥和呼吸窘迫��,肺部影像學(xué)上表現(xiàn)為非均一性的滲出性病變���,其發(fā)展至嚴(yán)重階段(氧合指數(shù)<200)被稱為急性呼吸窘迫綜合征(acuterespiratory distress syndrome,ARDS)�����。
根據(jù)治療指南[5]的流行病學(xué)調(diào)查顯示ALI/ARDS屬于臨床常見危重癥�。根據(jù)1994年歐美聯(lián)席會議提出的ALI/ARDS診斷標(biāo)準(zhǔn),ALI發(fā)病率為每年18/10萬����。2005年的研究顯示,ALI的發(fā)病率為每年79/10萬��,ARDS的發(fā)病率為每年59/10萬��。據(jù)此�,推測2030年國內(nèi)ALI/ARDS患者數(shù)將達(dá)200.8萬人����。ALI可導(dǎo)致肺泡上皮��、血管內(nèi)皮細(xì)胞損傷和肺血管通透性增加�����,主要臨床表現(xiàn)為低氧和�����、低肺順應(yīng)性和高生理死腔����,其病死率為30%-45%[6]。
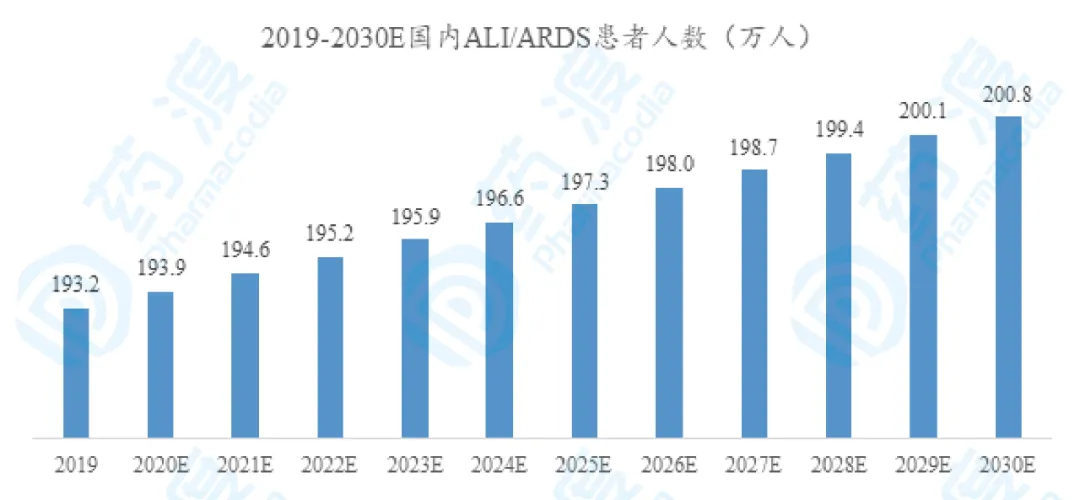
2019-2030E國內(nèi)ALI/ARDS患者人數(shù)(萬人)目前���,針對ALI的治療方式包括:原發(fā)病治療�、呼吸支持治療和藥物治療���。機(jī)械通氣是臨床上危重呼吸系統(tǒng)疾病的常用治療措施���,也是ALI的經(jīng)典治療方式���,然而,當(dāng)機(jī)械通氣達(dá)到10-15mL/kg較大潮氣量時����,可導(dǎo)致肺泡過度膨脹��,反而引起機(jī)械通氣相關(guān)性肺損傷[6]����。ALI患者病死率多年來居高不下,目前并無特效的治療藥物和方法���,在2020年之前�����,國內(nèi)一直無有效的治療藥物獲批上市��。注射用西維來司他鈉是全球唯一一個獲批用于治療ALI的藥物�,其屬于一種中性粒細(xì)胞彈性蛋白酶抑制劑�,主要是通過阻斷中性粒細(xì)胞介導(dǎo)的肺部炎癥反應(yīng)來治療ALI。西維來司他鈉的原研公司為日本小野制藥,原研藥于2002年4月11日在日本獲批上市���。另一方面�,2020年1月全國爆發(fā)COVID-19疫情��,并迅速蔓延至全球���,截至2020年6月24日����,全球確診COVID-19的病例數(shù)已經(jīng)達(dá)到918萬人�����,死亡人數(shù)達(dá)到47.5萬人��,致死率約為5.17%���。由COVID-19引起的肺損傷的治療也成為世界上亟待解決的關(guān)鍵問題�,中國通過27天的應(yīng)急審評審批����、現(xiàn)場檢查核查��,最終于2020年3月12日批準(zhǔn)了由上海匯倫江蘇藥業(yè)有限公司提出的可以治療ALI的藥物注射用西維來司他鈉的ANDA申請���。西維來司他鈉的年治療費用[7]為1.7萬元,目前ALI/ARDS治療以呼吸支持為主����,之前無有效治療藥物,但是藥物治療相對呼吸支持治療的護(hù)理費用更具有成本效益�,藥物治療可以降低費用,因此假設(shè)當(dāng)ALI/ARDS治療藥物增多時����,藥物治療占比為50%����,則預(yù)計2030年ALI/ARDS藥物市場規(guī)模將達(dá)170.7億元。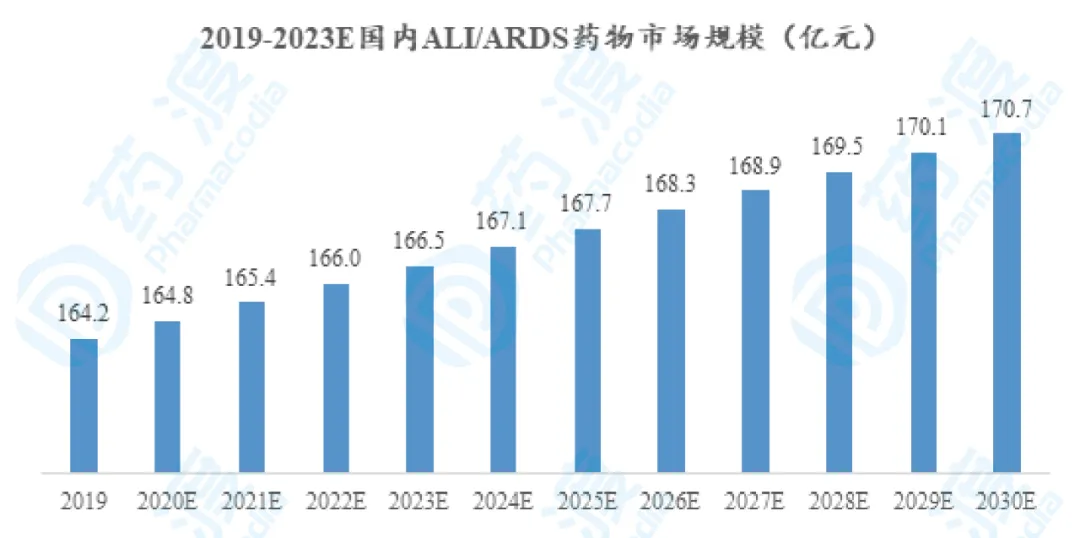
圖2-14 2019-2030E國內(nèi)ALI/ARDS藥物市場規(guī)模(億元)干眼是由于淚液的量或質(zhì)或流體動力學(xué)異常引起的淚膜不穩(wěn)定和(或)眼表損害���,從而導(dǎo)致眼不適癥狀及視功能障礙的一類疾病����。根據(jù)PeigeSong等人的Meta分析�,2010年中國5-89歲人群中,根據(jù)癥狀和體征分類的干眼癥的患病率為13.55%,患病人數(shù)為1.709億人[8]���。2018年全球眼科市場規(guī)模250億美元左右�����,其中干眼癥用藥占比15%��,市場規(guī)模約為37.5億美元[9]��。根據(jù)MarketScope預(yù)測�,2023年全球干眼癥市場規(guī)模將增長至62億美元[10]����。根據(jù)MarketScope分析,2019年中國眼科市場規(guī)模達(dá)到29億美元�����,干眼癥市場規(guī)模占到其中的7.5%�����,即2019年中國干眼癥市場規(guī)模約為2.18億美元����,合人民幣15.45億元[11]��。目前���,人工淚液是治療干眼癥的主要治療方案,我國主要使用的是玻璃酸鈉產(chǎn)品�。2018年玻璃酸鈉滴眼液在中國公立醫(yī)療機(jī)構(gòu)終端的銷售額為10.97億元[12]。中國干眼癥患者中已經(jīng)獲得治療的僅占一小部分�����,未來隨著干眼癥患者人群的進(jìn)一步增長以及治療率的進(jìn)一步提升���,中國干眼癥的市場規(guī)模將會進(jìn)一步擴(kuò)大。隨著Tβ4在分子水平的作用機(jī)制進(jìn)一步闡明和在臨床應(yīng)用研究不斷深入����,其臨床應(yīng)用價值將得到驗證,未來應(yīng)用前景值得期待���。